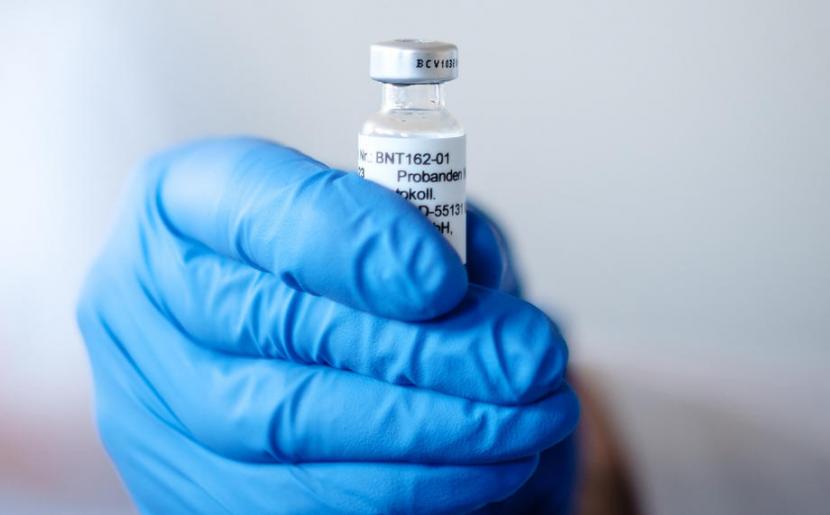
REPUBLIKA.CO.ID, JENEWA -- Organisasi Kesehatan Dunia (WHO) pada Rabu (2/12) mengatakan telah menerima data vaksin Covid-19 dari perusahaan Pfizer dan BioNTech dan kini sedang meninjaunya untuk "kemungkinan daftar penggunaan darurat" (EUL).
Prosedur Emergency Use Listing (EUL) merupakan patokan bagi negara-negara untuk mengesahkan penggunaan nasional. Merujuk pada regulator Inggris, Badan Regulasi Obat dan Kesehatan (MHRA), pihaknya melalui pernyataan mengatakan kepada Reuters, "WHO bersama dengan MHRA juga sedang membahas kemungkinan mengakses sejumlah informasi dari penilaian mereka, yang dapat mempercepat daftar penggunaan darurat WHO."
Inggris pada Rabu merestui vaksin Covid-19 Pfizer, melangkahi Amerika Serikat dan Eropa untuk menjadi negara Barat pertama yang secara resmi mendukung vaksin. Inggris menargetkan vaksin akan dapat menjangkau orang-orang yang paling rentan mulai awal pekan depan.
Pakar kedaruratan terkemuka WHO, Mike Ryan, menyambut baik kabar tersebut. Akan tetapi, ia menyebut pengembang vaksin lainnya harus tetap melanjutkan penelitian.
"Kita tidak boleh berhenti, kita membutuhkan lebih dari tiga sampai empat vaksin. Kita harus menggenjot produksi, kita harus menurunkan harga. Kita memerlukan vaksin satu dosis," katanya melalui acara media sosial.